食品藥物管理署(以下簡稱食藥署)為滿足國人用藥權益,針對國人生命及健康維護有迫切需求,或特定少數族群及特殊嚴重疾病之藥品,陸續公告多項藥品查驗登記的加速審查機制,包含精簡審查機制、優先審查機制、加速核准機制、突破性治療認定要點,以及小兒或少數嚴重疾病藥品審查認定要點等,目的在加速藥品查驗登記審查流程,縮短審查時間,以期新藥及早上市,嘉惠國人。
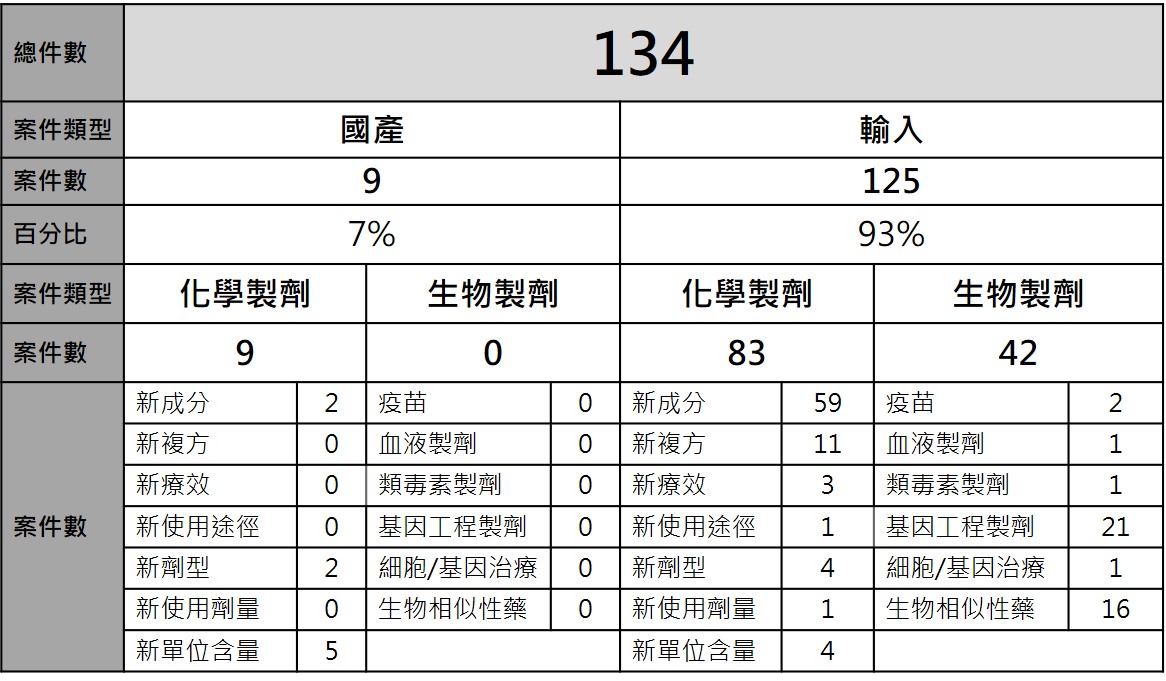
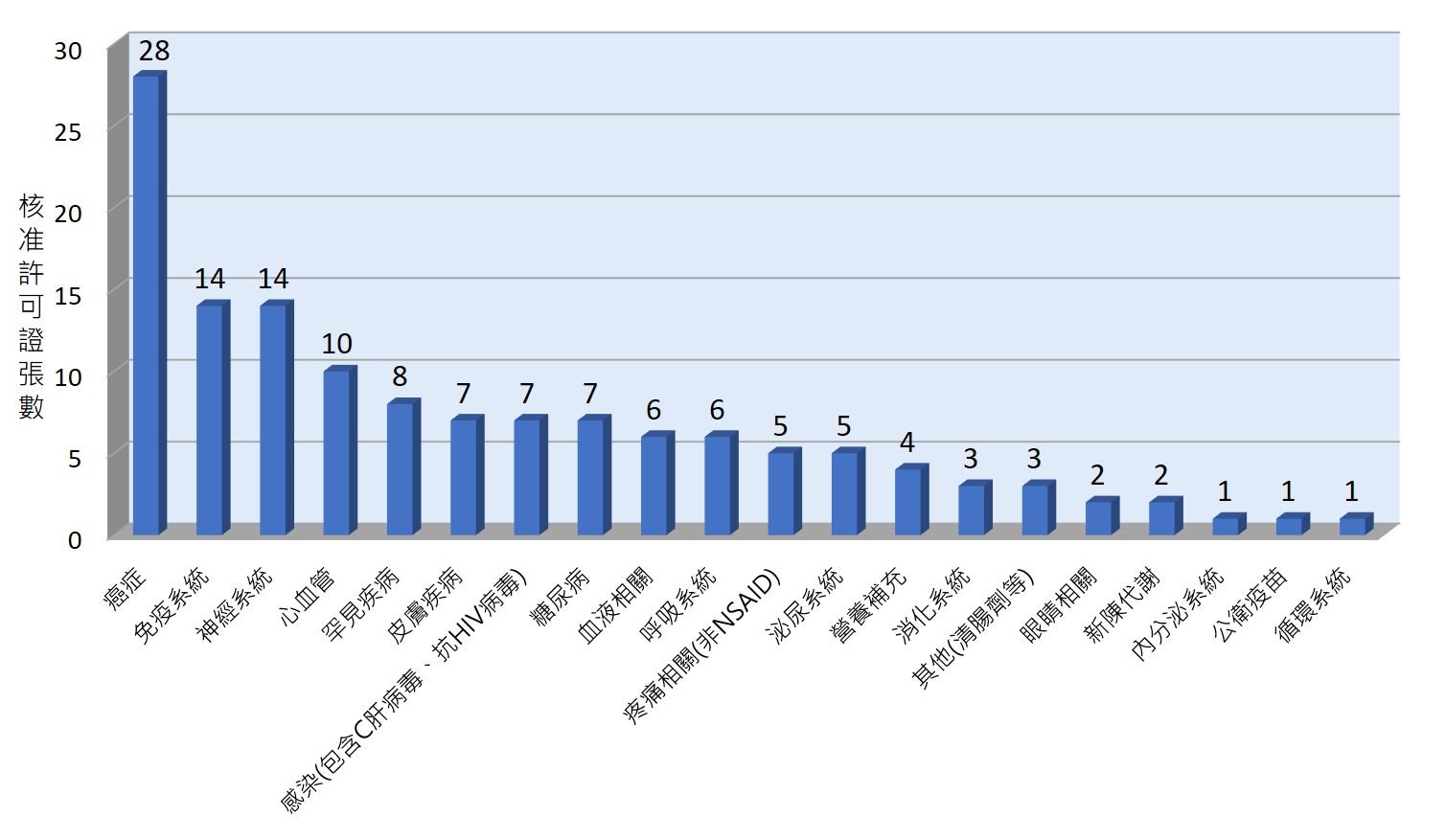
回顧110年度,食藥署核准134件的新成分新藥、新療效複方、新使用途徑、新劑型、新使用劑量、新單位含量藥品,其中9件為國產藥品,125件為輸入藥品;92件為化學藥品,42件為生物藥品,治療領域包括抗癌藥物、免疫系統藥物、神經系統藥物、心血管藥物、罕見疾病藥物等。前述諸多藥品採用藥品加速審查機制,審查天數由一般藥品360天大幅縮短至240天以下,顯示加速審查機制有效提高審查效率,並加速新藥上市。另,食藥署於110年度核准的一項標靶新成分新藥,即符合「少數嚴重疾病藥品審查認定要點」,透過加速審查流程,讓台灣繼美國FDA後成為亞洲第一個核准上市的國家,改善癌症病人的迫切需求,維護病人接受治療之權益。
食藥署為協助藥商全面性規劃藥品上市相關時程,陸續公告「藥品查驗登記退件機制查檢表」及「藥品審查流程及時間點管控表」,將我國藥品查驗登記案所需文件及審查流程透明化,強化案件審查時程的可預測性。另為鼓勵國際藥商於台灣執行多國多中心臨床試驗,於110年9月公告「鼓勵新成分新藥於國內執行臨床試驗試辦方案」,因應國際現況,彈性調整國內執行各期臨床試驗之受試者人數門檻,以期新藥及早來台,促使國人取得新穎藥品。食藥署將持續廣納業界意見,完善各項加速審查機制及鼓勵措施以符合實務現況,加速藥品上市,以滿足國人用藥權益,嘉惠國人。